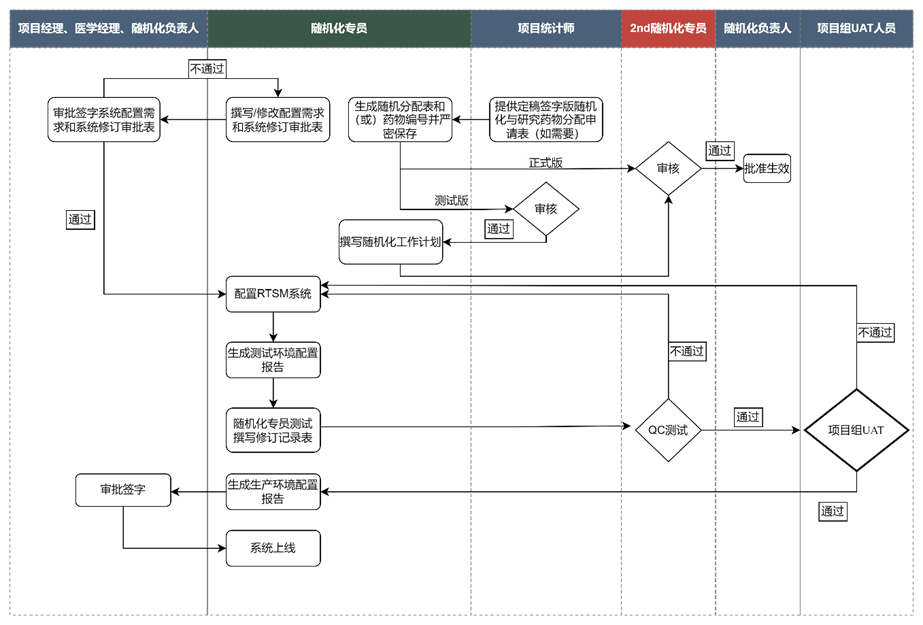
流程图
|
RTSM系统修订 SOP-CDSC-031 RTSM系统配置及修订 |
|
|
|
流程说明 |
|
|
流程说明
RTSM系统上线后修订
RTSM系统的修订需严格遵守修订流程。如方案变更,或其他原因需要修改RTSM系统时,随机化专员需结合系统的功能特点,评估修订的影响,提供 RTSM系统修订审批表。项目组需进行风险评估,审核并批准 SOP-CDSC-031F4_RTSM系统修订审批表。修订过程中相关文档需及时更新。
RTSM系统的修订主要包括组别变更、分层因素变更、治疗设计变更、访视变更。RTSM系统修订一般不包活系统用户管理、供应计划修订、提醒设定等。
随机化人员负责RTSM系统的修订,并在完成内部测试后通知项目组进行测试,收集测试问题并直至解决。 与修订相关的文件(RTSM系统使用手册等),如有需要,也需做相应的更新。RTSM中,修订前受试者已产生的数据应与修订后保持一致。
具体步骤如下:
- 随机化专员根据方案要求或项目需求,修订《SOP-CDSC-031F1 RTSM 系统配置需求》,提交《SOP-CDSC-031F4 RTSM系统修订审批表》;
- 项目经理、医学经理、随机化负责人审批签字修订后的《SOP-CDSC-031F1 RTSM 系统配置需求》,签字《SOP-CDSC-031F4 RTSM系统修订审批表》;
- 随机化专员根据定稿签字版《SOP-CDSC-031F1 RTSM 系统配置需求》配置RTSM系统;
- 项目统计师提供签字版《SOP-CDSC-030F1 随机化与研究药物分配申请表》;
- 随机化专员根据定稿签字版《SOP-CDSC-030F1 随机化与研究药物分配申请表》,使用随机化生成器生成测试版随机分配表和(或)药物编号表、正式版随机分配表和(或)药物编号表;
- 项目统计师审核测试版随机分配表与药物编号表,如审核不通过,随机化专员重新使用生成器生成随机分配表和(或)药物编号表,再发起测试版盲底文件审核;如审核通过,签字《SOP-CDSC-030F2 随机分配表和药物编号表审核表》;
- 随机化专员撰写并提供《SOP-CDSC-030F4_随机化工作计划》,2nd随机化专员审核并签署《SOP-CDSC-030F4_随机化工作计划》;
- 2nd随机化专员审核正式版随机分配表和(或)正式版药物编号表,如审核不通过,随机化专员重新生成随机分配表和(或)药物编号表,并发起审核。如审核通过,2nd随机化专员 签字《SOP-CDSC-030F3 随机分配表与药物编号表生效审批表》。随机化负责人批准并签字《SOP-CDSC-030F3 随机分配表与药物编号表生效审批表》。
- 随机化专员提供《SOP-CDSC-031F5 RTSM修订记录表》,2nd随机化专员审核并签署《SOP-CDSC-031F5 RTSM修订记录表》;
- 内部UAT(随机化专员测试),定稿签字《SOP-CDSC-031F6 RTSM系统随机化专员测试报告》;
- 项目组UAT(项目组用户测试):UAT前导出UAT环境的配置报告,定稿签字《SOP-CDSC-031F7 RTSM系统UAT报告》,定稿《XX项目_RTSM系统使用手册》;
- 随机化专员复制UAT环境配置至生产环境,导出生产环境的配置报告并与UAT环境配置报告进行比对,确认无误后填写《SOP-CDSC-031F2 RTSM系统配置报告签字页》及《SOP-CDSC-031F3 RTSM 系统上线使用签字页》。
- 项目经理、医学经理、随机化负责人确认并签署生产环境的《SOP-CDSC-031F2 RTSM系统配置报告签字页》及《SOP-CDSC-031F3 RTSM 系统上线使用签字页》。
注:以上文件可根据项目需求决定是否更新。
以上步骤可参考随机化工作其他流程节点的说明。
CDTMS填写要求
- RTSM系统的修订需严格遵守修订流程。如方案变更,或其他原因需要修改RTSM系统时,随机化专员需结合系统的功能特点,评估修订的影响,提供 RTSM系统修订审批表。项目组需进行风险评估,审核并批准 SOP-CDSC-031F4_RTSM系统修订审批表。修订过程中相关文档需及时更新。
- RTSM系统的修订主要包括组别变更、分层因素变更、治疗设计变更、访视变更。RTSM系统修订一般不包活系统用户管理、供应计划修订、提醒设定等。
- 随机化人员负责RTSM系统的修订,并在完成内部测试后通知项目组进行测试,收集测试问题并直至解决。 与修订相关的文件(RTSM系统使用手册等),如有需要,也需做相应的更新。RTSM中,修订前受试者已产生的数据应与修订后保持一致。
- 人工填写字段:
- “计划开始日期”、 “计划完成日期”、“修订原因”、“备注”;
- 自动生成文件:
- “修订计划”:以上信息保存后;